Son biomoléculas formadas por cadenas lineales de aminoácidos.
Por sus propiedades físico-químicas, las proteínas se pueden clasificar en proteínas simples (holoproteidos), formadas solo por aminoácidoso sus derivados; proteínas conjugadas (heteroproteidos), formadas por aminoácidos acompañados de sustancias diversas, y proteínas derivadas, sustancias formadas por desnaturalizacion y desdoblamiento de las anteriores.
Funciones
- Contráctil (actina y miosina)
- enziatica (Ej.:sacaroza y pepsina)
- Estructural. Esta es la función más importante de una proteína (Ej.:colageno)
- Homeostática: colaboran en el mantenimiento del ph (ya que actúan como un tampon quimico)
- Inmunológica (anticuerpos)
- Producción de costras (Ej.:fibrina)
- Protectora o defensiva (Ej.: trombina y fibrogeno)
- Transducción de señales (Ej.: rodopsina).
- La actina y miosina, responsables finales del acortamiento del muculo durante la contracción
- Los anticuerpos , encargados de acciones de defensa natural contra infecciones o agentes patógenos
- Funciones de reserva. Como la ovoalbúmina en el huevo, o la caseina de la leche
- El colageno, integrante de fibras altamente resistentes en tejidos de sosten
- Casi todas las enzimas y catalizadores de reacciones químicas en organismos vivientes
- La hemoglobina y otras moleculas con funciones de transporte en la sangre
- Muchas hormonas, reguladores de actividades celulares
- Los receptores de las células, a los cuales se fijan moléculas capaces de desencadenar una respuesta determinada.
Estructura
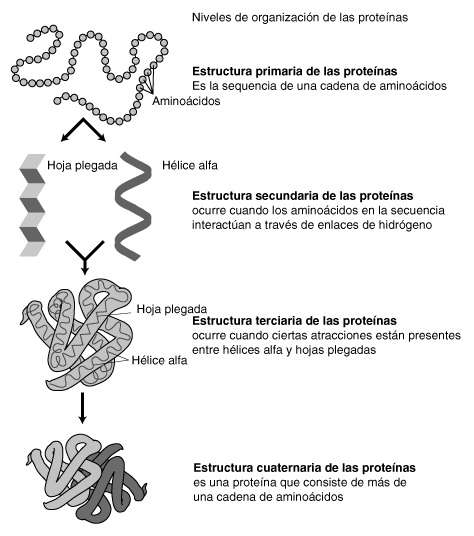
Propiedades
- Amortiguadores del ph (conocido como efecto tampon): Actúan como amortiguadores de pH debido a su carácter anfótero, es decir, pueden comportarse como ácidos (donando electrones) o como bases (aceptando electrones).
- Capacidad electrolítica: Se determina a través de la electroforesis, técnica analítica en la cual si las proteínas se trasladan al polo positivo es porque su molécula tiene carga negativa y viceversa.
- Especificidad : Cada proteína tiene una función específica que está determinada por su estructura primaria.
- Estabilidad: La proteína debe ser estable en el medio donde desempeñe su función. Para ello, la mayoría de proteínas acuosas crean un núcleo hidrofóbico empaquetado. Está relacionado con su vida media y el recambio proteico.
- Solubilidad: Es necesario solvatar la proteína, lo cual se consigue exponiendo residuos de similar grado de polaridad al medio en la superficie proteica. Se mantiene siempre y cuando los enlaces fuertes y débiles estén presentes. Si se aumenta la temperatura y el ph se pierde la solubilidad.
Clasificación
Según su forma
-
- Fibrosas: presentan cadenas polipeptídicas largas y una estructura secundaria atípica. Son insolubles en agua y en disoluciones acuosas. Algunos ejemplos de éstas son queratina colágeno y fibrina.
-
- Globulares: se caracterizan por doblar sus cadenas en una forma esférica apretada o compacta dejando grupos hidrófobos hacia adentro de la proteína y grupos hidrófilos hacia afuera, lo que hace que sean solubles en disolventes polares como el agua. La mayoría de las enzimas, anticuerpos, algunas hormonas y proteínas de transporte, son ejemplos de proteínas globulares.
-
- Mixtas: posee una parte fibrilar (comúnmente en el centro de la proteína) y otra parte globular (en los extremos).
Segun su composición química
- Simples u holoproteínas: en suhidrolisis solo produce aminoácidos. Ejemplos de estas son la insulina y el colageno (globulares y fibrosas), albuminas, proteína simple
- Conjugadas o heteroproteínas: estas proteínas contienen cadenas polipeptídicas y un grupo prostético. La porción no aminoacídica se denomina grupo prostético, estos pueden ser un ácido nucleico, un lípido, un azúcar o ion inorgánico.